2014年2月13日
味の素株式会社(社長:伊藤雅俊 本社:東京都中央区)は、京都大学iPS細胞研究所(以下、京大CiRA所長:山中伸弥教授)と共同で、再生医療を想定し、動物・ヒト由来の成分を含まないより安全性の高いiPS/ES細胞用の培地「StemFit®」AK03の開発に成功しました。また、当社は、この成果を活かし、世界初のiPS細胞を用いた網膜再生医療による治療を目指す株式会社ヘリオス(社長:鍵本忠尚 本社:東京都中央区)に、この培地を提供します。
○長期培養が可能な、より安全性の高い培地の開発に成功
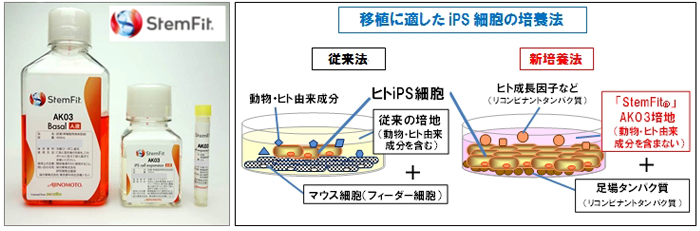
当社は、iPS細胞を用いた再生医療の実現を目指し、京大CiRAの中川誠人講師と2011年からiPS細胞を培養する培地に関する共同研究を行ってきました。培地とは、細胞を生育させ増やすための栄養液で、iPS細胞は、これまで、ウシの血清を含む培地を用い、フィーダー細胞と呼ばれるマウス(ネズミの一種)の細胞と混ぜた状態で培養する方法が用いられていました。
このたび、当社の分析・配合技術と京大CiRAのiPS細胞に関する知見・研究成果を組み合わせ、培養に必須の因子を最適な比率で配合することにより、iPS細胞およびES細胞を長期にわたり安定的に増殖することが可能な「StemFit®」AK03培地の開発に成功しました。この培地は、再生医療に使うことを想定し、バイオ技術で作成したリコンビナントタンパク質を利用することにより、動物やヒトに由来する成分を全く含まず、精製された成分のみで構成されています。
○PMDAの対面助言を受ける
「StemFit®」AK03培地の安全性に関し、厚生労働省の薬事審査機関である独立行政法人医薬品医療機器総合機構(PMDA)の対面助言を受けたところ、「生物由来原料基準」を適用する原料は含んでいないことが確認されました。この確認は安全性の視点で重要だと考えています。
○世界初のiPS細胞を用いた再生医療の研究開発に活用
当社は、この「StemFit®」AK03培地を京大CiRAに提供しています。また、理化学研究所 高橋政代先生と協働して、世界で初めてiPS細胞由来の網膜色素上皮細胞の移植による加齢黄斑変性の新たな治療法の研究・開発をしている株式会社ヘリオスにも提供する予定です。当社は、今後、この培地の開発・工業化を進め、2016年に販売を開始する予定です。その後の再生医療の拡大に伴い、2025年には「StemFit®」AK03をはじめとする再生医療用培地のグローバルでの売上げ400億円を目指します。
味の素グループは、iPS細胞やES細胞の培養に用いる「StemFit®」培地の販売を通じて、再生医療の実現や新しい医薬品の開発に寄与することにより、人類の健康な生活の実現に貢献していきます。
参考資料
<株式会社ヘリオス 概要>
用語説明
iPS細胞(induced pluripotent stem cell:人工多能性幹細胞)
ヒトの皮膚などの体細胞に、極少数の遺伝子などを導入することにより、様々な組織や臓器の細胞に分化する能力と、ほぼ無限に増殖する能力をもつ多能性幹細胞のこと。
ES細胞(embryonic stem cell)
受精後6、7日目の胚盤胞から細胞を取り出して培養することにより作られた多能性幹細胞のこと。あらゆる組織の細胞に分化することができる。
リコンビナントタンパク質
バイオ技術により、微生物や酵母などを用いて作り出したタンパク質のこと。バイオ医薬品として、がんやリウマチの治療薬など、広く用いられている。
生物由来原料基準
「医薬品等」に使用される人その他の生物(植物を除く)に由来する原料又は材料について、製造に使用される際に講ずべき必要な措置に関する基準。(平成15年厚生労働省告示第210号)
報道関係の方向けお問い合わせ先はこちら
|
||||||||||||||||||
| 閉じる |